北京天悦生科技有限公司
8 年
手机商铺
- NaN
- 0
- 0
- 0
- 0
推荐产品
技术资料/正文
8月必看的干细胞研究进展!
168 人阅读发布时间:2019-09-09 11:07
近期,中国科学院动物研究所曲静研究组和中国科学院生物物理研究所刘光慧研究组合作,在Nature Communications在线发表研究论文,首次报道了miRNA合成通路关键因子DGCR8通过稳固异染色质抑制人间充质干细胞衰老的新型生物学功能,为延缓器官衰老、防治衰老相关疾病提供了新型潜在干预靶标。
DGCR8作为经典miRNA合成通路中的关键蛋白,广泛参与非编码RNA合成、mRNA可变剪接和转录后调控等重要生物学过程,但其在干细胞衰老中的调控作用尚不明确。在该项研究中,研究人员利用CRISPR/Cas9介导的基因编辑技术和干细胞定向诱导分化技术,获得DGCR8功能缺陷型人间充质干细胞,并观察到这些细胞出现加速衰老的表型。进一步研究发现,DGCR8可与核膜蛋白Lamin B1以及异染色质蛋白KAP1和HP1形成复合物,共同参与维持异染色质结构的稳定性,从而保持人间充质干细胞的年轻态。此外,在复制性衰老、生理性衰老以及早衰症加速衰老的人间充质干细胞中,DGCR8的表达水平均发生下调,而过表达野生型的DGCR8或miRNA加工活性缺失的DGCR8突变体均可有效延缓人间充质干细胞的衰老。更重要的是,基于DGCR8过表达的基因治疗可有效抑制小鼠关节组织衰老,促进关节软骨再生,缓解损伤性骨关节炎及衰老性骨关节炎的病理表型。
该研究首次确立了DGCR8通过稳定异染色质结构调节人间充质干细胞的稳态和衰老的新功能,并揭示了以DGCR8为靶标的骨关节炎基因治疗新路径。这是继近期两个研究组合作揭示干细胞“年轻因子”CBX4和“年轻通路”YAP-FOXD1后骨关节炎基因治疗领域的又一创新性发现。这些研究结果均证明通过基因疗法导入“干细胞去衰老因子”治疗骨关节炎的可行性,具有潜在的临床应用价值。
该研究工作由中科院动物所、生物物理所、干细胞与再生医学创新研究院以及首都医科大学宣武医院等机构合作完成,曲静和刘光慧为共同通讯作者。该项目得到科技部、国家自然科学基金委、中科院战略性先导科技专项等的支持。
2.TEPCM:磁性间充质干细胞有望改善机体的软骨修复
近日,一项刊登在国际杂志Tissue Engineering Part C:Methods上题为“In Vitro Safety and Quality of Magnetically Labeled Human Mesenchymal Stem Cells Preparation for Cartilage Repair”的研究报告中,来自日本广岛大学的科学家们通过研究评估了这种磁性标记的间充质干细胞(MSCs)在修复软骨缺陷上的安全性和有效性。
研究者Naosuke Kamei博士表示,这项研究中我们通过核型分析、克隆形成实验和总增殖实验证明了磁性标记的MSCs的安全性,在标记后我们仅发现了间充质干细胞的微小差异。研究人员能通过软骨细胞的分化及其对磁力的反应性来评价干细胞的质量,研究结果表明,适宜浓度的超顺磁性氧化铁纳米颗粒在保证磁性吸引力的同时,还有助于优化间充质干细胞的分化能力。
最后,该杂志的主编,来自拉德堡德大学医学中心的教授John A. Jansen表示,将间充质干细胞精准化地运输到机体缺损部位或是利用这种干细胞进行组织再生研究和应用的重要一步。
Hiroshi Negi et al, In Vitro Safety and Quality of Magnetically Labeled Human Mesenchymal Stem Cells Preparation for Cartilage Repair, Tissue Engineering Part C: Methods (2019). DOI: 10.1089/ten.tec.2019.0001
3.Science子刊:对特定的造血干细胞亚群进行CRISPR-Cas9基因编辑可有效逆转多种血液疾病的症状
在一项新的研究中,来自美国弗雷德哈钦森癌症研究中心等研究机构的研究人员利用CRISPR-Cas9对长寿的造血干细胞进行编辑,从而逆转在包括镰状细胞病和β地中海贫血在内的几种血液疾病中观察到的临床症状。这是科学家们首次对成体造血干细胞中的一个特定亚群的遗传组成进行特异性编辑,其中造血干细胞是血液和免疫系统中所有细胞的来源。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Therapeutically relevant engraftment of a CRISPR-Cas9–edited HSC-enriched population with HbF reactivation in nonhuman primates”。
这项原理验证研究表明对靶向干细胞进行高效修饰可能会降低血液疾病和其他疾病的基因编辑治疗成本,同时降低可能产生的副作用的风险。
论文共同第一作者、Kiem实验室研究员Olivier Humbert博士说道,“鉴于CRISPR技术仍处于早期开发阶段,证实我们的方法是安全的是比较重要的。我们在经过编辑的细胞中并未发现有害的脱靶突变,而且我们当前正在进行长期随访研究以验证没有任何不良影响的发生。”
这是第一项特异性地对一小部分造血干细胞进行编辑的研究,Kiem团队在2017年发现这部分造血干细胞完全负责再生完整的血液和免疫系统。为了区分,Kiem团队将这一部分造血干细胞称为CD90细胞,这是根据蛋白标志物CD90命名的,这种蛋白标志物可让CD90细胞与其余的造血干细胞(携带另一种蛋白标志物:CD34)区别开来。
这种干细胞群体的自我更新特性使得它们成为进行基因治疗的强大潜在候选者,这是因为它们能够长期地产生这些经过基因修饰的血细胞,从而可以在一生当中治疗疾病。鉴于它们仅占所有造血干细胞的5%,因此利用基因编辑复合物靶向它们将需要更少的供应和潜在更低的成本。
Olivier Humbert et al. Therapeutically relevant engraftment of a CRISPR-Cas9–edited HSC-enriched population with HbF reactivation in nonhuman primates. Science Translational Medicine, 2019, doi:10.1126/scitranslmed.aaw3768.
4.Science子刊:靶向嘧啶合成增强胶质母细胞瘤干细胞的分子治疗反应
胶质母细胞瘤是一种侵入周围脑组织的恶性脑癌,手术治疗极为困难。即使化疗和放疗成功地摧毁了患者大部分胶质母细胞瘤细胞,它们也可能不会影响癌症干细胞。这一小群肿瘤细胞有无限增长和繁殖的能力,并能导致肿瘤复发。
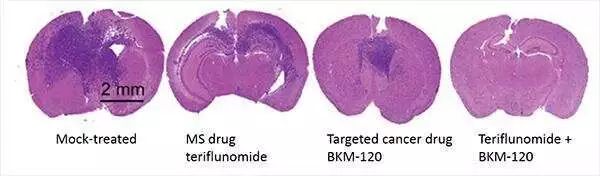
为了研究这些肿瘤并测试新的治疗方法,加州大学圣地亚哥医学院的研究人员使用了携带手术患者捐献的胶质母细胞瘤肿瘤样本的老鼠。通过这种方法,他们最近发现,联合靶向癌症治疗和多发性硬化症(MS)药物特立氟胺治疗可以阻断胶质母细胞瘤干细胞,显着缩小肿瘤,提高小鼠存活率。这项研究发表在2019年8月7日的《Science Translational Medicine》上。
近年来,个性化癌症治疗的愿望导致了几种靶向癌症治疗的发展。这些药物通过抑制癌细胞赖以生长和生存的特定分子发挥作用。因此,与传统疗法(如化疗和放疗)相比,靶向治疗效果更好,副作用更少。然而,靶向治疗并没有像科学界所希望的那样成功。Rich认为,这是因为仅仅抑制一个驱动肿瘤形成或存活的分子或通路通常是不够的--癌细胞会找到一种补偿方式。
为了继续复制,胶质母细胞瘤干细胞需要不断制造更多的DNA,而要做到这一点,它们需要制造嘧啶,这是DNA的组成部分之一。Rich的团队从6个不同的数据库中挖掘了数百名胶质母细胞瘤患者的肿瘤基因组数据,发现嘧啶代谢分数越高,患者存活率越低。
MS药物特立氟胺恰好能阻断嘧啶形成酶。Rich和他的团队在实验室中发现特立氟胺抑制胶质母细胞瘤细胞的存活、自我更新和肿瘤的发生。更重要的是,研究人员发现,与接受模拟治疗的小鼠相比,单独使用特立氟胺治疗时,患者产生的肿瘤略有缩小,携带肿瘤的小鼠存活时间有所延长。
研究小组还测试了两种靶向癌症疗法:BKM-120和拉帕替尼。BKM-120是一种抑制剂,在缺乏PTEN酶驱动的胶质母细胞瘤细胞中效果最好;拉帕替尼是一种抑制剂,用于治疗表皮生长因子受体(EGFR)突变驱动的癌症。单独使用BKM-120治疗后,与接受模拟治疗或特立氟胺治疗的小鼠相比,肿瘤适度缩小,小鼠存活时间更长。
但同时使用特立氟胺和BKM-120治疗后,与接受模拟治疗的小鼠和单独接受两种治疗的小鼠相比,肿瘤平均显着缩小,小鼠存活时间显着延长。
Xiuxing Wang et al. Targeting pyrimidine synthesis accentuates molecular therapy response in glioblastoma stem cells, Science Translational Medicine (2019). DOI:10.1126/scitranslmed.aau4972
5.Circulation:科学家有望利用干细胞衍生的心肌细胞来修复受损的心脏!

近日,一项刊登在国际杂志Circulation上的研究报告中,来自阿拉巴马大学伯明翰分校的科学家们通过研究开发了一种新方法,其或能利用干细胞衍生的心肌细胞来改善心脏病的修复;心脏病发作后会引发部分肌肉壁死亡,从而就会使心脏无法再生,死亡的组织会压迫周围的肌肉导致患者出现致命性的心脏扩张。
生物医学工程师认为,通过利用多能干细胞在体外培养心肌细胞,随后将这些心肌细胞或这些细胞制成的“贴片”置于死亡的心脏组织位点,就能够有效修复衰竭的心脏,基于这种方法的实验和临床试验证据也能够改善心脏左心室的泵送能力。然而,通过移植细胞来改善心脏的供血以及心脏的功能或许取决于这些细胞的质量,研究人员面临的一大挑战就是这些细胞的移植率较低。
这项研究中,研究人员开发了一种新方法来改善所移植细胞的质量,他们表示,在心脏病小鼠模型中进行试验后发现,注射的干细胞衍生的心肌细胞的移植率提高了一倍,这种新方法能够在异质群体中选择功能完整且DNA完整的细胞,从而使其能够适应临床状况,更好地重建缺血的心肌组织并改善衰竭心脏的功能表现。心脏细胞的移植需要数百万的干细胞或其衍生细胞,在加速状况下的细胞繁殖是获取大量细胞的常用手段,但加速生长也会造成培养的压力,包括致死性的DNA损伤,这些DNA损伤的细胞或许无法适用于细胞移植。
研究者表示,他们能够激活诱导多能干细胞中的转录因子p53从而选择性地诱导程序性细胞死亡(细胞凋亡)发生,尤其是DNA损伤的细胞,同时还会保留DNA未发生损伤的细胞;研究者利用MDM2抑制剂(Nutlin-3a)能够激活p53的表达,当进行Nutlin-3a疗法后,死亡的细胞就会从培养液中被洗掉,剩下的DNA未受到损伤的细胞则会正常生长并分化为心肌细胞;随后研究者将90万个衍生的心肌细胞注射到了心脏病小鼠模型心脏左心室的边界区域,四周后,研究者发现,接受DNA未发生损伤的心肌细胞的心脏中植入率发生了明显提高(大约14%),而对照衍生的心肌细胞的植入率则约为7%。
研究者Kannappan表示,这项研究中我们首次发现,在诱导多能干细胞培养液中通过激活p53就能够有效选择DNA未发生损伤的诱导多能干细胞,而且这些DNA未发生损伤的心肌细胞还能够增强心脏移植的潜力。此前研究结果表明,DNA损伤的衰老细胞并不会经历细胞死亡,相反其会停留在组织内部,并伴随功能的改变,从而改变组织的微环境促进其它细胞老化,这或许是DNA未受损伤的心肌细胞拥有移植优势的一种解释。
研究者指出,这种移除DNA损伤细胞的方法具有广泛的应用价值;这种新方法能够利用小分子来选择DNA损伤的细胞,尽管研究者需要优化和评估其它选择性条件,但这种方法能用于任何类型的干细胞,而治疗多种疾病的干细胞疗法或许也会因为采用这种新方法而获益,包括神经变性疾病、大脑和脊髓损伤等。
Ramaswamy Kannappan,James F. Turner,Jessica M. Miller, et al. Functionally Competent DNA Damage-Free Induced Pluripotent Stem Cell–Derived Cardiomyocytes for Myocardial Repair, Circulation (2019). DOI:10.1161/CIRCULATIONAHA.119.040881
6.Nature子刊:人胚胎干细胞衍生的心外膜细胞在3D心脏中经过测试

根据英国心脏基金会(BHF)资助并在Nature Biotechnology上发表的一项新研究,人胚胎干细胞(hESC)衍生的心外膜细胞可能是开发心力衰竭治疗方法。
英国成千上万的人通常因心脏病发作而患有心力衰竭。心力衰竭(heart failure)简称心衰,是指由于心脏的收缩功能和(或)舒张功能发生障碍,不能将静脉回心血量充分排出心脏,导致静脉系统血液淤积,动脉系统血液灌注不足,从而引起心脏循环障碍症候群,此种障碍症候群集中表现为肺淤血、腔静脉淤血。心力衰竭并不是一个独立的疾病,而是心脏疾病发展的终末阶段。
据文献报道,人胚胎干细胞(hESC)衍生的心外膜被证明在体外增强工程心脏组织的结构和功能,并提高了hESC-心肌细胞移植物在梗塞的无胸腺大鼠心脏中的功效。与间充质基质细胞相比,心外膜细胞显着增强人工程心脏组织的收缩性,肌原纤维结构等。移植的心外膜细胞在梗塞心脏中形成持久性成纤维细胞移植物。hESC衍生的心外膜细胞和心肌细胞的共移植使体内移植物心肌细胞增殖率加倍,心脏移植物大小增加6倍,同时增加移植物和宿主血管形成。
值得注意的是,与单独接受心肌细胞或单独接受心外膜细胞的心脏相比,它们的组合共移植改善了收缩功能。也就是,通过心脏肌细胞和心壁外层支持细胞的组合移植受损组织区域,它们可以帮助器官从心脏病发作的损伤中恢复过来。
科学家们多年来一直试图用干细胞修复受损的心脏。到目前为止,一直没有成功,主要是因为绝大多数移植细胞在几天内死亡。
现在,剑桥大学的Sanjay Sinha博士和他的团队与华盛顿大学的研究人员合作,使用人类干细胞培养的心外膜细胞来帮助移植心脏细胞在体内存活时间更长。
研究人员使用人体干细胞在实验室培养的3D人类心脏组织来测试细胞组合的效果,发现心外膜细胞帮助心肌细胞生长和成熟。它们还改善了心肌细胞收缩和放松的能力。
在心脏受损的大鼠中,该组合还帮助移植的细胞存活并恢复失去的心肌和血管细胞。
现在,研究人员希望了解支持性心外膜细胞如何帮助促进心脏再生。了解这些关键细节将使他们更接近在临床试验中测试心脏再生疗法。
患有心力衰竭的人不能再生受损的心脏,唯一的治疗方法就是心脏移植。最终,这些研究人员希望,通过利用干细胞的再生能力,他们终有一天能够使用患者自己的细胞来治愈人类的心脏。
除BHF外,该研究由英国医学研究委员会(MRC)和国家健康研究所(NIHR)资助。
BHF资助的研究员兼剑桥大学研究负责人Sanjay Sinha博士说:“英国有成千上万的人患有心力衰竭,许多人正在与时间赛跑进行挽救生命的心脏移植手术。但是在英国每年只进行大约200次心脏移植手术,这对我们来说寻找替代疗法尤为必要。”
7.Nat Biotechnol:人类胚胎干细胞来源的心外膜细胞增强心肌细胞驱动的心脏再生
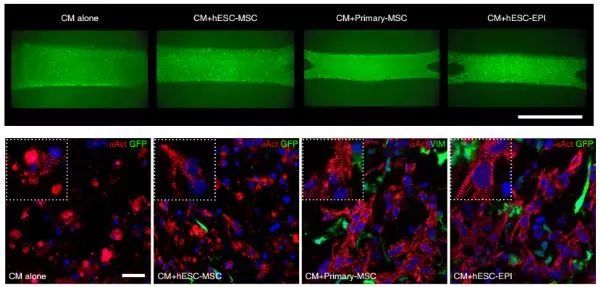
心外膜及其衍生物为发育和成体心脏提供营养和结构支持。为此,来自华盛顿大学的Charles E. Murry和剑桥大学的Sanjay Sinha合作测试了人类胚胎干细胞(hESC)来源的心外膜在体外增强工程心脏组织的结构和功能的能力,并提高hESC-心肌细胞移植在心肌梗死大鼠心脏中的疗效。相关研究成果发表在《Nature Biotechnology》上,题为"Epicardial cells derived from human embryonic stem cells augment cardiomyocyte-driven heart regeneration"。
与间充质间质细胞相比,心外膜细胞显着增强了人工程心脏组织的收缩力、肌原纤维结构和钙处理能力,减少了被动刚度。移植的心外膜细胞在梗死的心脏中形成持久的成纤维细胞移植物。hESC来源的心外膜细胞和心肌细胞在体内的联合移植使移植物心肌细胞的增殖速度增加了一倍,使心脏移植物的尺寸增加了2.6倍,同时增强了移植物和宿主的血管化。
值得注意的是,与单独接受心肌细胞、心外膜细胞或载体的心脏相比,联合移植改善了心脏的收缩功能。
因此,该研究表明心外膜细胞增强心脏移植物体积和功能的能力使其成为一种有希望的心脏修复辅助治疗手段。
Sanjay Sinha et al. Epicardial cells derived from human embryonic stem cells augment cardiomyocyte-driven heart regeneration. Nature Biotechnology volume 37, pages895-906 (2019). DOI https://doi.org/10.1038/s41587-019-0197-9
8.Stem Cells Dev:美国科学家发布诱导多能干细胞成熟性的标准研究指南

研究人员开发了一个指南,帮助实验室标准化从干细胞中产生成熟的类肝细胞(hepatic-like cells,HPCs)的方法,并将HPCs的基因表达与实际人体肝脏组织进行比较。这种中度的高通量的方案可以相对快速地评估干细胞分化的有效性,并有助于指导再生医学应用中分化条件的优化。该操作指南及其影响发表在《Stem Cells and Development》杂志上。
这个名为"Guide to the Assessment of Mature Liver Gene Expression in Stem Cell-Derived Hepatocytes"的指南由卡罗林斯卡医学院的Stephen Strom、匹兹堡大学的Alejandro Soto-Gutierrez以及来自伊朗干细胞生物学研究所的同事共同撰写。研究人员使用实时定量聚合酶链反应(rt-qPCR)检测了60多个基因在胎儿和成熟人类肝脏样本中的mRNA表达情况,并将其归一化为内参。他们测量了自己实验室和从商业实验室购买的iPCs中的基因表达。评估的基因包括肝脏特异性血浆蛋白、细胞色素P450酶、转运体、多药耐药蛋白的基因,以及多能性和iPCs分化为不同细胞类型的能力的基因。
Stem Cells and Development杂志主编、来自密西根州底特律韦恩州立大学医学院Carman and Ann Adams儿科的Graham C. Parker说道:"能够引导干细胞群向目标成熟的细胞类型分化的能力和演示这一过程的持久性和有效性仍然是大多数干细胞生物学家无法完成的事情,而且更令人担忧的是这一领域继续忍受着一些没有证据的论文。在这项具有里程碑意义的论文中,Stephen Strom和他的同事为其他实验室提供了一个基准技术,来比较他们的干细胞来源的类肝细胞和实际的人类肝脏样本。"
Mihaela Zabulica et al, Guide to the Assessment of Mature Liver Gene Expression in Stem Cell-Derived Hepatocytes, Stem Cells and Development (2019). DOI:10.1089/scd.2019.0064





