北京唯尚立德生物科技有限公司
入驻年限:5 年
- 联系人:
孙博士
- 所在地区:
北京 昌平区
- 业务范围:
技术服务、试剂、耗材、论文服务、细胞库 / 细胞培养、体外诊断
- 经营模式:
生产厂商 科研机构
推荐产品
公司新闻/正文
Runx2 通过调节 Itgav 的转录表达激活肝星状细胞来促进肝的纤维化
人阅读 发布时间:2023-09-01 10:08

方法和结果
在这项研究中,研究人员发现 Runx2 的表达在不同病因所形成的人类肝纤维化中都显著上调。在纤维化过程中 Runx2 在小鼠肝脏中的表达也逐渐升高,并且 Runx2 主要在活化的 HSC 中表达。在 HSC 中 Runx2 的敲除显著减轻了 CCl4, DDC or MCD 诱导的肝纤维化,而通过对小鼠的肝进行 HBAAV-Runx2 或 VA-Lip-Runx2 的注射过表达 Runx2 加剧了 CCl4 诱导的肝纤维变性。体外的分析表明 Runx2 促进了 HSC 的活化和增殖,而在 HSC 中敲低 Runx2 则抑制了这些作用。通过 RNA-seq 和 Runx2-ChIP-seq 的分析表明 Runx2 可以通过结合启动子来促进 Itgav 基因的表达。阻断 Itgav 则可减弱 Runx2 诱导的 HSC 活化和肝纤维化。此外,研究还发现细胞因子 TGF-β1, PDGF and EGF 可以通过蛋白激酶 A(PKA)来促进 HSC 中 Runx2 的表达和核转位。
结论转录因子 Runx2 在肝纤维化过程中通过转录调节 Itgav 的表达,对 HSC 的活化至关重要,它可能是肝纤维化的一个比较有前途的治疗靶点。1. 在肝纤维化进展的过程中 Runx2 的表达逐渐增加为了研究 Runx2 在肝纤维化中的作用,研究人员首先在 GEO 数据库中探索了 Runx2 的表达。在由不同病因引起的肝硬化患者中 Runx2 的表达要高得多,如酒精性肝病、病毒性肝炎和 NAFLD(图 1 A)。研究人员还发现 Runx2 的表达水平在晚期纤维化患者中较高,而在早期纤维化患者中较低,这表明 Runx2 的表达在肝纤维化的进展过程中会增加。接着,研究人员从非纤维化和肝硬化患者的身上收集人类肝组织,结果也显示 Runx2 的蛋白和 mRNA 水平在肝硬化患者的肝组织中显著上调(图 1 B and C)。组织学分析马松染色显示肝硬化组织中胶原严重沉积,同时 Runx2 and α-SMA(活化 HSC 的标志物)表达显著增加。在纤维索处 Runx2 也呈阳性染色(图 1 D)。在 GEO 数据库和 CCl4 引起的小鼠纤维化模型中,在纤维化的肝组织中也观察到了类似的 Runx2 表达上调的结果(图 1 E-H)。更重要的是,研究人员发现 Runx2 and α-SMA 在高脂饮食诱导的非酒精性脂肪性肝炎(NASH)相关的肝纤维化中均显著增加(图 1 H)。
为了进一步研究 Runx2 在肝纤维化过程中的表达趋势,研究人员用 CCl4 处理小鼠 1 周和 6 周以诱导肝的损伤和纤维化,并监测 Runx2 的表达。研究发现,随着肝损伤的持续,胶原沉积逐渐增加,在受损肝脏中 α-SMA and Runx2 的表达轻度上调,但在纤维化肝脏中明显增加,这与 GEO 数据库的分析一致。有趣的是,组织学染色结果表明 Runx2 的阳性染色主要分布在肝组织的纤维索和间隔中,与 α-SMA 阳性细胞的分布一致(图 1 D and H)。总之,这些发现表明 Runx2 的表达在肝纤维化过程中逐渐增加,并在肝组织中表现出潜在的细胞特异性表达的特征。
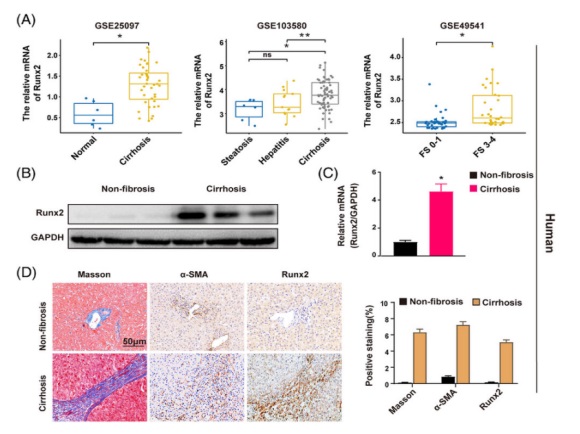

fig.1
2. Runx2 在体内特异性定位于活化的 HSC 中,并在体外 HSC 活化的过程中以时间依赖性的方式增加表达
由于 Runx2 主要在肝间质细胞中表达,与 α-SMA 的表达一致,研究人员在纤维化的小鼠肝脏中用 α-SMA(活化的 HSC 标记物), CD31(内皮细胞标记物) 和 F4/80(库普弗细胞标志物)对 Runx2 进行共染,以评估 Runx2 在肝脏中表达空间的特异性。正如预测的那样,仅在 Runx2 和 α-SMA 之间观察到共表达的现象,这在人类肝硬化的肝组织中得到了进一步证实(图 2 A)。此外,通过比较静态的和从 CCl4 处理 4 周的小鼠中分离的活化的 HSC 之间的 Runx2 表达,发现活化 HSC 中 Runx2 的表达显著增加(图 2 B)。值得注意的是,单细胞 RNA 测序分析显示,与早期培养的原代 HSC 相比 Runx2 在肌成纤维细胞(分化良好的 HSC)中高度表达和分布,这与肌纤维细胞标记物(α-SMA and Col1a1)一致,这进一步支持 Runx2 主要存在于活化的 HSC 中(图 2 C)。最重要的是,在 HSC 的激活过程中 Runx2 的 mRNA 和蛋白表达以时间依赖性的方式进行上调,这与纤维化基因的表达有关,包括 α-SMA, collagen I and TGF-β1(图 2 D and E)。同时,研究人员还观察到 Runx2 在体外表现出过度的核转位并伴有 HSC 活化,这意味着 Runx2 同时开始了其转录功能(图 2 F)。总之,这些结果表明 Runx2 在活化的 HSC 中特异性表达,并可能在调节 HSC 活化中发挥作用。

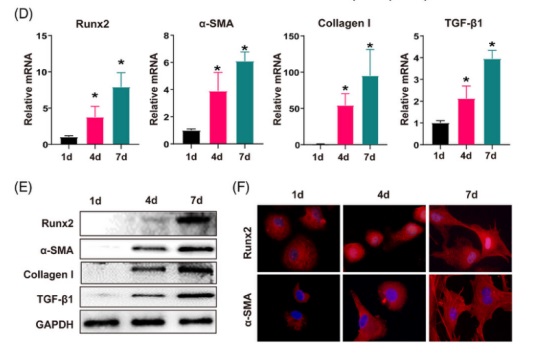
fig.2
3. HSC 特异性敲低 Runx2 可以减轻 CCl4, DDC and MCD 诱导的小鼠肝纤维化为了确定 Runx2 在体内肝纤维化过程中的作用,研究人员首先使用慢病毒介导的 shRNA 在 CCl4 和橄榄油对照诱导的小鼠中敲低了 Runx2 数据表明敲低 Runx2 减轻了 CCl4 诱导的肝纤维化。接下来,研究人员又通过使用 PDGFRβ-Cre(HSC 特异性基因) 小鼠来构建出了 HSC 特异性敲除 Runx2 基因的小鼠。然而,纯合子(Runx2ff;PDGFRα-Cre)在出生后立即死亡,因此 Runx2 半敲除的杂合子小鼠(Runx2f+;PDGFRβ-Cre or Runx2△+HSC)被用于进一步的体内研究(图 3 A)。结果表明,在 CCl4 诱导的纤维化组中 Runx2 的敲低降低了促纤维化基因,包括 TGF-β1, collagen I and α-SMA 的 mRNA 和蛋白水平的表达。尽管它们的 mRNA 表达水平在用橄榄油处理的 Runx2△+HSC 小鼠中轻度下降,但这些基因的蛋白质水平没有显示出显著的变化(图 3 B and C)。此外,敲低 Runx2 在组织学上显著减轻了 CCl4 诱导的肝纤维化,减少了 I 型胶原的沉积和 HSC 的活化(图 3 D)。此外,研究人员还建立了DDC or MCD 诱导的肝纤维化小鼠模型,以评估 Runx2 在其他病因引起的肝纤维化中的作用。通过 H&E 染色证实 DDC 或 MCD 成功在小鼠中诱导了胆汁淤积症和 NASH, 另外,与对照组相比 Runx2 敲除小鼠的纤维化和 HSC 的激活水平都显著降低(图 3 E)。类似地 Runx2 的敲降也降低了 DDC and MCD 诱导的纤维化肝组织中 I 型胶原和 α-SMA 的 mRNA 和蛋白质的表达。此外,由于肝细胞(HC)损伤是肝纤维化的一个组成部分,研究人员通过使 Runx2ff 小鼠与 Alb-Cre 小鼠来进行繁育也构建了 HC 特异性敲除 Runx2 的小鼠(Runx2△/△HCs)来验证在 HC 中的 Runx2 敲除是否会影响肝纤维化的进展。不出所料 Runx2 的 HC 特异性敲除并不会影响 CCl4 诱导的肝纤维化。总之,这些发现表明 HSC 中 Runx2 的敲除减轻了 CCl4, DDC and MCD 诱导的肝纤维化。
fig.3
4. Runx2 的过表达加剧了 CCl4 诱导的肝纤维化为了进一步证实 Runx2 在肝纤维化中的作用,研究人员通过注射 HBAAV-Runx2 三周来构建 Runx2 过表达小鼠,然后又用橄榄油和 CCl4 来处理小鼠 4 周(图 4 A)。随后,分离原代 HSC 和 HC 并检测 Runx2 基因 mRNA 的表达,以弄清过表达质粒在肝不同细胞群间的递送和表达效率。结果显示,与 HSC 相比,大多数 HBAAV-Runx2 被转染到了 HC 中。然而,由于 Runx2如前所述并没有影响 HC, 因此在某种程度上研究人员成功地构建了在 HSC 中过表达 Runx2 的小鼠。在使用 CCl4 处理后,结果发现,与对照组相比,在 HBAAV-Runx2 过表达小鼠中 Runx2, collagen I and α-SMA 的 mRNA 和蛋白的表达都显著增加(图 4 B and C)。在组织学上,与对照组相比,过表达 HBAAV-Runx2 组小鼠的肝脏结构表现出广泛的结构紊乱和相邻血管间显著的间隙(图 4 D)。在 HBAAV-Runx2 小鼠中 I 型胶原和 α-SMA 细胞的阳性染色也增加,表明纤维化严重,大量 HSC 被激活(图 4 D)。此外,研究人员发现在橄榄油处理的小鼠中 Runx2 的过表达触发了 GFAP 阳性细胞(静态 HSC)的增殖,但不影响胶原沉积, HSC 的活化, I 型胶原和 α-SMA 的 mRNA 和蛋白的表达(图 4 D),这表明 Runx2 在 HSC 中的过表达不能触发自发纤维化或 HSC 活化。此外,研究发现,通过注射携带 Runx2(VA-Lip-Runx2) 或 VA-Lip-Ctrl 质粒的脂质体,在 HSC 中特异性过表达 Runx2 增强了 CCl4 诱导的小鼠肝纤维化。综上所述,这些结果表明 Runx2 的过表达会加剧 CCl4 诱导的肝纤维化。
fig.4
5. Runx2 在体外调节 HSC 的激活由于 Runx2f/f 小鼠与 PDGFRβ-Cre 小鼠只能培育出 Runx2 半敲除的杂合子小鼠(Runx2△/+HSC);研究人员利用 GFAP-Cre(肝中 HSC 的另一种标记物)小鼠与 Runx2f/f 小鼠杂交,成功获得 Runx2 敲除纯合子小鼠(Runx2△/△HSC)(图 5 A)。考虑到 GFAP-Cre 也可以标记胆管细胞,所以 Runx2△/△HSC 小鼠在本次研究中主要被用于进行体外实验。为了进一步评估 Runx2 在 HSC 激活中的作用,从 Runx2△/△HSC 和 HBAAV-Runx2 小鼠中分离出原发性 HSC 并培养 4 天(图 5 B)。结果发现在 Runx2△/△HSC 小鼠缺失 Runx2 基因的 HSC 中 HSC 标记基因和纤维化基因,如 desmin, α-SMA, Col1a1, Col3a1, MMP2, MMP9, MMP13, TIMP-1, TGF-β1 和 PDGFRβ 的 mRNA 表达都降低了(图 5 C),并且 α-SMA, collagen I and TGF-β1 的蛋白表达也降低了(图 5 D),然而在 Runx2 过表达小鼠的 HSC 中,纤维化基因如 α-SMA, collagen I and TGF-β1 的 mRNA 和蛋白的表达都提高了(图 5 E and F)。此外 Runx2 缺失抑制了 α-SMA 的表达,并在体外维持了 HSC 静态的表型(图 5 I)。接着,研究人员进一步使用小干扰 RNA 来敲低原代 HSC, LX2(人 HSC 细胞系)和 mHSC (小鼠 HSC 细胞系)中的 Runx2. 结果显示 Runx2 缺失降低了所有细胞中 α-SMA mRNA 的表达,而 Runx2 过表达上调了 mHSC 细胞中 α-SMA mRNA 的表达。此外,流式细胞分析的结果显示 Runx2 的敲除显著减少了 HSC 的 G2 期,表明 HSC 增殖受到抑制,但 Runx2 的过表达会持续导致 HSC 细胞 S 期的减少和 G2 期的增加,并显著促进了 HSC 在体外的生长(图 5 G),这表明 Runx2 是 HSC 增殖的正向调节因子。总之,这些发现表明 Runx2 是 HSC 激活和增殖的重要转录因子。
fig.5
6 .Itgav 是 Runx2 在肝纤维化中的直接下游靶点为了探索 Runx2 调节 HSC 激活的潜在机制,研究人员通过使用转染了干扰 Runx2 表达的 siRNA 的原代 HSC 来进行 RNA 测序(RNA-seq)。根据 KEGG 富集分析的结果显示 Runx2 敲低主要与激活 HSC 的信号通路受损有关,包括凋亡、细胞周期、自噬、MAPK and TGF-β 信号通路(图 6 A)。由于 Runx2 在各种生物过程中起转录因子的作用,所以研究人员对来自 HBAAV-Runx2 小鼠的 HSC 又进行了染色质免疫沉淀测序(ChIP-seq)分析,以确定 Runx2 在活化的 HSC 中的直接靶点。结果显示 Runx2 与许多 DNA 序列有结合,其中许多峰位于靶基因的转录起始位点附近。根据 KEGG 分析发现 Runx2 结合的区域主要靠近 PI3K-Akt 信号通路、代谢通路、TGF-β 信号通路等相关基因(图 6 B)。进一步 RNA-seq and ChIP-seq 显示 Runx2 对 TGF-β 信号通路有显著影响。然而,包括 TGF-β1 在内的 TGF-β 配体并不是 Runx2 的直接下游因子,这表明 Runx2 可能通过不直接介导 TGF-β 配体的表达的方式来调节 TGF-β 信号通路。由于 TGF-β 信号通路是调节 HSC 活化和肝纤维化过程中最重要的通路之一,整合 TGF-β 通路相关基因转录组和 ChIP-seq 数据集,获得了 7 个常见基因,包括 Itgav, Thbs1, Lox, Src, Spry2, Smad7 和 Npnt(图 6 C)。其中 Itgav 基因编码了 αv 整合素的主要成分,而 αv 整合素是调节 TGF-β1 激活和肝纤维化进展的关键整合素,这表明 Runx2 可能是通过 Itgav 信号通路来激活 HSC 的。使用 ChIP-seq 分析发现 Runx2 与 Itgav 转录起始位点上游的 Chr2:8372357-83723806 结合,这种结合通过荧光素酶报告基因测定实验得到了证实(图 6 D and E)。此外,对来自 Runx2△/△HSC, Runx2△/+HSC 和 HBAAV-Runx2 小鼠的肝组织和原代 HSC 中 Itgav 基因的 mRNA 和蛋白表达进行了检查,结果表明 Runx2 缺乏或过表达在体外和体内降低或增加了 Itgav 的表达(图 6 F-I)。鉴于 Itgav 与 ECM 配体结合并激活下游激酶,包括 FAK and PI3K. 以及与 TGF-β1 相互作用以激活 TGF-β1 信号通路。因此,研究人员检测了来自 Runx2 敲除和过表达小鼠原代 HSC 中的磷酸化 FAK, PI3K and Smad2/3 的表达。结果表明,磷酸化 FAK, PI3K and Smad2/3 的表达在 Runx2 过表达的 HSC 中增强,而在 Runx2 敲除的 HSC 则降低(图 6 I)。总之,我们的研究结果强烈表明 Runx2 通过与 Itgav 启动子结合来直接上调 Itgav 的表达,并激活潜在的信号转导,这反过来又有助于 HSC 的激活和肝纤维化的进展。同时,相关分析显示 Runx2 与 Itgav (r=.98), TGF-β1(r=.91) 和 collagen I(r=.97)高度相关。且 Itgav 也与 TGF-β2(r=.87) and collagen I(r=0.94)高度相关。这些结果表明,这些基因之间可能存在一些功能关系,它们可能共同调节或参与相似的生物通路。
fig.6
7 .抑制 αv 整合素阻断了 Runx2 过表达引起的 CCl4 诱导的肝纤维化加重为了探索 Itgav 在 Runx2 相关 HSC 激活和肝纤维化中的作用,研究人员首先通过在从HBAAV-ctrl 和 HBAAV-Runx2 小鼠中分离出的原代 HSC 中使用小干扰 RNA 来沉默 Itgav 基因,结构显示 Itgav 敲低显著阻断了 Runx2 过表达诱导的 α-SMA 上调。由于 Itgav 编码的整合素 α-V 链是五种 αV 整合素的主要成分,其表达变化将影响所有五种 αV 整合素的功能,因此,研究人员进一步利用 αv 整合素的小分子抑制剂(CWHM-12)来确定 Itgav 介导的 αv 整合素功能是否确实在 HSC 激活和肝纤维化进展中处于 Runx2 调节的下游(图 7 A)。结果发现 αv 整合素抑制显著阻断了 Runx2 过表达引起的 α-SMA 上调,这与 siItgav 相似(图 7 B and C)。然后,给 HBAAV-Runx2 或 HBAAV-ctrl 小鼠注射 CCl4 诱导 2 周以构建肝纤维化,然后再给药 CWHM-12 或 DMSO 处理 2 周(图 7 D)。结果显示 CWHM-12 显著降低了 α-SMA 的 mRNA 和蛋白质表达,并阻断了 Runx2 诱导的 α-SMA 表达上调,这与体外数据一致(图 7 E and F)。在组织学检测中,通过胶原沉积(Masson and collagen I 染色)和 α-SMA 染色检测显示 CWHM-12 显著减少了肝纤维化,重要的是抑制 αv 整合素显著阻断了 Runx2 加重的肝纤维化(图 7 G)。研究人员还通过在小鼠中同步静脉注射携带 Itgav siRNA 的脂质体(VA-Lip-siItgav) 和 VA-Lip-Runx2 来特异性阻断 Itgav 在 HSC 中的表达,以避免 CWHM-12 可能潜在的副作用,结果显示 siItgav 也显著抑制了 Runx2 促进的肝纤维化。因此,研究结果表明 Runx2 主要通过 Itgav 激活 HSC 并促进肝纤维化。
fig.7
8 .在 HSC 中 Runx2 的激活和核转位受 PKA 的调节Runx2 从细胞质到细胞核的易位是其转录活性所必需的。因此,研究人员也试图找出提高 Runx2 表达并控制其易位进入细胞核的上游调节信号。研究表明,蛋白激酶 A(PKA)激活 Runx2 并在肠上皮细胞的上皮-间质转化和成骨细胞分化过程中介导其核转位。此外 PKA 也是 PDGF, EGF 和 TGF-β1 的常见下游激酶,它们是调节 HSC 激活的必需细胞因子。因此,研究人员利用 TGF-β1, PDGF-BB 或 EGF 来激活使用或不用 PKA 抑制剂(PKI-6-22)处理的原代 HSC 细胞。结果显示 TGF-β1, PDGF-BB 和 EGF 都显著增加了 Runx2 的表达,而 PKA 抑制剂则消除了这效应(图 8 A)。此外 Runx2 可以激活 Itgav 的转录,因此也检测了 PKA 对 Itgav 的影响。结果显示 TGF-β1, PDGF-BB 和 EGF 显著增加了 Itgav 的表达,但所有这些也都被 PKA 抑制剂消除了(图 8 A)。此外,研究还发现 PKA 激活剂(8-Bromo-cAMP)可以刺激 Runx2 在 HSC 中的核分布。相反 PKA 抑制剂在有或没有 TGF-β1 培养的 HSC 中减弱了 Runx2 的核转位(图 8 B)。免疫荧光染色还表明,用 PKA 抑制剂处理的 HSC 导致了细胞核中 Runx2 的表达受到了抑制,使得 HSC 表型保持更加静止,而 PKA 激活剂诱导了 Runx2 在细胞核中的分布更高并且使得 HSC 活化(图 8 C)。总之,这些发现表明 TGF-β1, PDGF-BB 或 EGF 通过 PKA 激活 Runx2 并促进其核转位。
fig.8





