NEJM 官方翻译 | 美国首例新冠病毒肺炎治疗康复全过程
北京时间 2020 年 2 月 1 日凌晨,《新英格兰医学杂志》(NEJM)在短篇报告栏目(Brief Report)报道了美国首例确诊新型冠状病毒肺炎患者成功治愈的病例。读者亦可访问 www.nejm.org/coronavirus,阅读英文;或访问 nejmqianyan.cn,阅读中文。
这是 NEJM 中文版《NEJM 医学前沿》第 5 篇全文翻译 NEJM 发表的 2019-nCoV 文章。我们希望通过官方全文翻译让读者全面了解论文信息。疫情当前,更需要冷静分析,独立判断。
此外,关于本研究所用抗病毒药物,其生产商吉利德公司的官方声明指出,remdesivir 尚未在全球任何地区获得许可或批准,也尚未证明其任何用途的安全性或疗效,此例治疗是在无任何已批准治疗方案前提下的紧急方案。
致敬奋战在抗击疫情一线的医护、疾控和后勤保障人员!祝你们平安凯旋!
特别致谢翻译团队侯琦,何群,范齐文,颜婷茹上海嘉会国际医院实验室
 图片来源:NEJM
图片来源:NEJM
概述
一种新型冠状病毒(2019-nCoV)在中国武汉暴发,传播迅速,目前已在多个国家出现确诊病例。
我们报告了在美国确诊的第一例 2019-nCoV 感染病例,并描述了该病例的鉴别、诊断、临床病程和治疗,包括此患者最初的轻微症状及在发病第 9 日进展为肺炎。
这一病例突出了临床医师与当地、州和国家各级公共卫生机构密切协调的重要性,以及快速发布突发感染患者相关临床信息的必要性。
2019 年 12 月 31 日,中国报道了一个与湖北省武汉市华南海鲜批发市场相关的肺炎病例集群 [1]。2020 年 1 月 7 日,中国卫生机构确认此病例集群与一种新型冠状病毒 2019-nCoV 相关 [2]。虽然最初报告的病例与武汉海鲜市场暴露相关,但目前的流行病学数据表明,2019-nCoV 正在发生人际传播 [3-6]。
截至 2020 年 1 月 30 日,至少 21 个国家已报告了 9976 例确诊病例,其中包括美国在 2020 年 1 月 20 日报告的第一例 2019-nCoV 感染确诊病例 [7]。
目前正在全球范围内展开调查,以便更好地了解其传播动力学和临床疾病谱。本报告描述了美国第一例 2019-nCoV 感染的流行病学和临床特征。
病例报告
2020 年 1 月 19 日,一名 35 岁男性来到华盛顿州斯诺霍米什县的急诊诊所,他有 4 天咳嗽和自觉发热病史。
患者一进诊所,就在候诊室里戴上了口罩。等待大约 20 分钟后,他被带进了检查室,并接受了医师评估。
患者透露,他曾在中国武汉探亲,于 1 月 15 日返回华盛顿州。患者说,他看到了美国疾病控制和预防中心(CDC)关于中国新型冠状病毒暴发的健康警报,鉴于他的症状和最近的旅行史,决定来看医师。
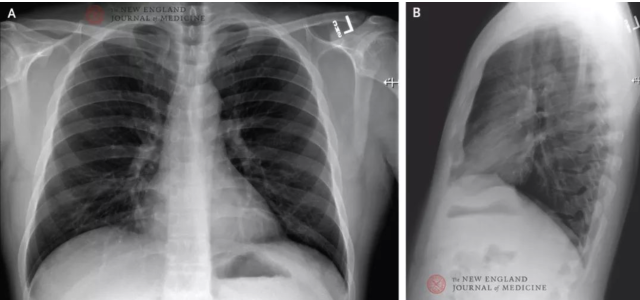
图 1. 后前位和侧位胸片,2020 年 1 月 19 日(发病第 4 日)。无胸部基础疾病。
图片来源:NEJM
除有高血脂病史外,该患者不吸烟者且平素健康。体格检查:体温为 37.2°C,血压为 134/87 mm Hg,脉搏为 110 /分,呼吸为 16 次/分,患者呼吸环境空气时的氧饱和度为 96%。
由于肺部听诊出现干啰音,故进行胸片检查,结果为未见异常(见图 1)。
快速核酸扩增检测(NAAT)显示甲型和乙型流感抗原呈阴性。取鼻咽拭子用 NAAT 进行呼吸道病毒的病原体检测;48 小时后报告所有检测病原体结果为阴性,包括甲型和乙型流感病毒、副流感病毒、呼吸道合胞病毒、鼻病毒、腺病毒和 4 个可以致人类发病的冠状病毒(HKU1、NL63、229E、OC43)。
基于患者旅行史,医生立即上报地方和国家相关卫生管理部门。汇同急诊医师,华盛顿卫生健康部立即报告了美国 CDC 应急管理中心。
尽管患者表示没有去过武汉海鲜市场且在华旅行期间也没有接触过任何病患,但 CDC 工作人员依据目前的 CDC「需调查人员」病例定义,一致同意对该患者进行 2019-nCov 检测 [8]。我们按 CDC 指南对患者进行了样本采集,包括血清、鼻咽拭子、口咽拭子样本。样本采集后,对患者进行了在当地卫机构的监控下的居家隔离。
2020 年 1 月 20 日,CDC 证实通过采用实时逆转录酶聚合酶链检测方法(rRT-PCR),该患者鼻咽拭子和口咽拭子 2019 新型冠状病毒(2019-nCov)检测结果为阳性。
通过与美国 CDC 相关专家,国家和当地的健康官员,急诊医疗中心,医院管理层和员工的通力合作,该患者被收治进入普罗维登斯医疗中心的隔离病房进行医学观察,医务人员按照 CDC 建议进行了相应防护(包括眼部防护),以防止接触,飞沫,气溶胶等污染 [9]。
收治入院后,患者出现了持续性干咳,恶心和呕吐 2 天;患者自诉无呼吸困难和胸痛,且生命体征都在正常范围内。体格检查发现患者出现粘膜干燥,其他检查没有明显异常。
住院后,对患者进行了支持治疗,包括 2 L 的生理盐水静滴和昂丹司琼缓解恶心症状。
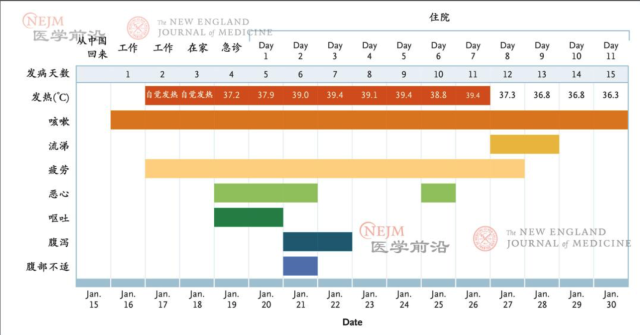
图 2. 按照患者发病及住院日期(2020 年 1 月 16 日至 2020 年 1 月 30 日)列出的症状和最高体温。
图片来源:NEJM
住院第 2 至 5 日(发病第 6 至 9 日),除出现间歇性发热并伴有心动过速之外,患者生命体征基本平稳。患者仍有干咳,乏力。住院第 2 日下午,患者排稀便,腹部不适。夜间再次排稀便;采集的粪便和上呼吸道样本,以及鼻咽和口咽拭子经 rRT-PCR 检测 2019-nCoV 均呈阳性,血清检测为阴性。
自此期间,主要对患者实施支持性治疗。对患者给予对症治疗:根据发热情况给予退热药,包括每 4 小时 650 mg 对乙酰氨基酚和每 6 小时 600 mg 布洛芬;口服 600 mg 愈创甘油醚缓解持续咳嗽;住院后 6 天内大约给予 6 L 生理盐水补液。
由于患者隔离病房最初只允许用床旁设备进行样本检测,患者住院第 3 日才开始全血细胞计数及血清化学检测。
在患者住院的第 3 日开始进行血常规和生化检测。患者住院第 3 日和第 5 日(发病第 7 日和第 9 日)实验室结果显示:白细胞减少,轻度血小板减少以及肌酸激酶(CK)水平升高(表 1)。此外,肝功能指标也出现异常:ALKP(68 U/L),ALT(105 U/L),AST(77 U/L)和 LDH(465 U/L)的水平都在住院的第 5 日所有升高。
鉴于患者反复发热,在住院第 4 日进行了血培养检测,截至目前未有细菌生长。
患者住院第 3 日(发病第 7 日)的胸片检查显示没有肺部浸润或其他异常(图 3)。然而,在住院第 5 日晚上(发病第 9 日)的第二次胸片显示左下肺叶有肺炎迹象(图 4)。
以上影像学的发现与患者住院第 5 日晚上开始的呼吸症状改变相吻合,该患者当日呼吸环境空气时的氧饱和度下降至 90%。住院第 6 日给患者行 2 L/分鼻导管吸氧。
考虑到临床表现的突然变化和发生医院获得性肺炎的可能性,给予万古霉素(1750 mg,然后每 8 小时静脉注射 1 g)和头孢吡肟(每 8 小时静脉注射一次)治疗。
表 1. 临床实验室结果。
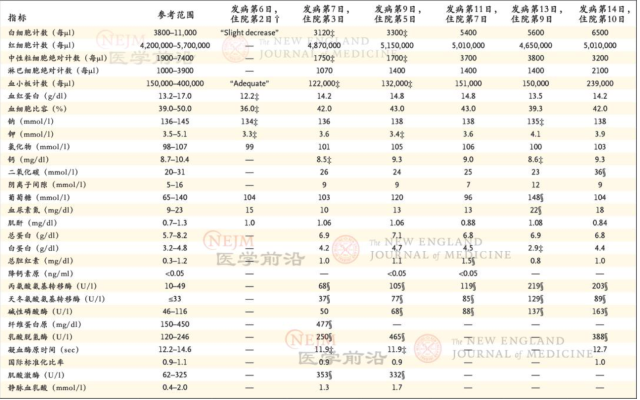
将钙值转换成 mmol/L 需乘以 0.250。将血尿素氮值转换为 mmol/L 需乘以 0.357。将肌酸酐值转换为 μmol/L 需乘以 88.4。将总胆红素值转换为 μmol/L 需乘以 17.1. 结果来自 POCT 血气分析仪(iSTAT).‡患者血液分析结果低于正常值。§患者血液分析结果高于正常值。
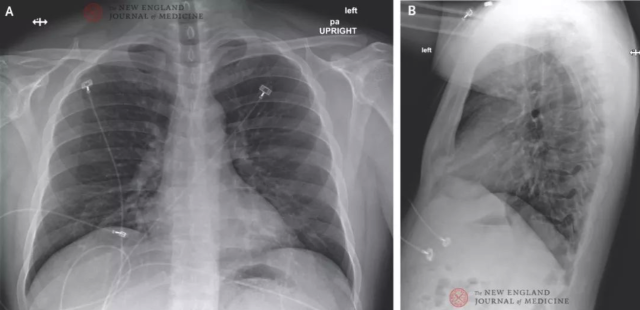
图 3. 后前位及侧位胸片,2020 年 1 月 22 日 (发病第 7 日,住院第 3 日)。胸内片平扫无异常提示。
图片来源:NEJM
在患者住院第 6 日(发病第 10 日),第 4 次胸片检查显示双下肺条索状阴影。胸片结果与不典型肺炎诊断吻合(图 5),双肺听诊提示有水泡音。
根据患者的影像学检查结果,开始吸氧的治疗决策,患者的持续发热,多个样本的 2019-nCoV RNA 持续阳性结果,以及有报道指出其他患者在与该患者的影像学肺炎一致的时间段发生重度肺炎 [3,4],因此临床医师将一种试验性抗病毒药进行了特许用药。
住院第 7 日晚上,这名患者接受了 remdesivir(一种处于研发阶段的核苷酸类似物 [10,11])静脉输注,无明显副作用。第 7 日晚上,得到连续阴性的降钙素原水平和耐甲氧西林金黄色葡萄球菌 PCR 阴性结果后,停用万古霉素,第 8 日停用头孢吡肟。
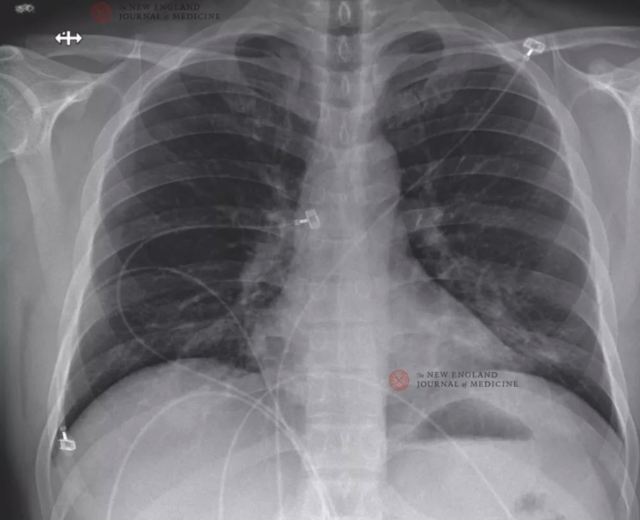
图 4. 2020 年 1 月 24 日后前位胸片(发病第 9 日,住院第 5 日)。左肺下叶毛玻璃样改变加重,提示肺炎可能。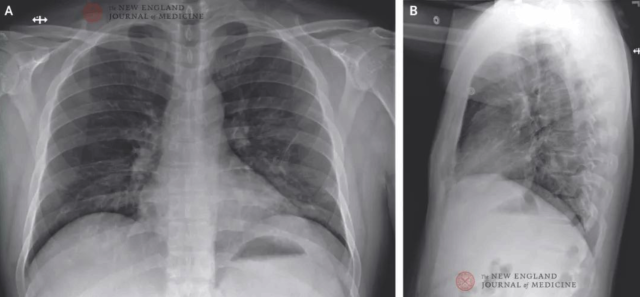
图 5. 正位胸片和侧位胸片,2020 年 1 月 26 日(发病第 10 日,住院第 6 日)。肺叶底部呈持续毛玻璃样斑点,提示可能为非典型肺炎;毛玻璃样改变随时间推移不断增强。
在住院第 8 日(发病第 12 日),患者临床症状得到改善。停止了吸氧治疗,患者呼吸环境空气时的氧饱和度也提高到 94~96%。之前双下肺的水泡音也消失。患者食欲也出现好转,除了间歇性干咳和流涕外,无其他临床症状。
截止 2020 年 1 月 30 日,患者还在住院治疗。但无发热,除咳嗽改善比较缓慢外,所有其他临床症状均消退。
方法
样本采集
用于 2019-nCoV 诊断检测的临床样本是依照美国 CDC 指南采集 [12]。鼻咽和口咽拭子样本是采用合成纤维拭子采集;每个拭子被放入装有 2~3 ml 病毒运送培养液的单独无菌试管中。
血清被采集到血清分离管中,然后依照美国 CDC 指南离心。尿液和粪便样本分别采集到无菌样本容器内。运送到美国 CDC 之前,样本在 2°C~8°C 保存。用于重复 2019-nCoV 检测的样本是在发病第 11 和 12 日采集,包括鼻咽和口咽拭子、血清、尿液和粪便样本。
2019-nCoV 的诊断检测
临床样本是通过根据公开病毒序列开发的 rRT-PCR 检测法进行检测。与之前严重急性呼吸综合征冠状病毒(SARS-CoV)和中东呼吸综合征冠状病毒(MERS-CoV)的诊断检测法相似,2019-nCoV 的诊断检测法包括 3 个核衣壳基因靶点和一个阳性对照靶点。关于该检测法的说明 [13] 及 rRT-PCR 引物和探针 [14] 的序列的信息参见关于 2019-nCoV 的美国 CDC 实验室信息网站 [15]。
基因测序
2020 年 1 月 7 日,中国研究人员在美国国立卫生研究院 GenBank 数据库 [16] 和「全球流感数据共享计划」(Global Initiative on Sharing All Influenza Data,GISAID)[17] 数据库共享了 2019-nCoV 的完整基因序列;之后又发表了关于分离 2019-nCoV 的报告 [18]。
核酸是从 rRT-PCR 阳性样本(口咽部和鼻咽部)提取出,并在桑格和二代测序平台(Illumina 和 MinIon)进行了全基因组测序。序列组装采用的是 5.4.6 版 Sequencer 软件(Sanger);2.17 版 minimap 软件(MiniON)和 1.3.1 版 freebayes 软件(MiSeq)。将完整基因组与已发布的 2019-nCoV 参考序列(GenBank 登录号 NC_045512.2)进行了比较。
表 2. 2019 新型冠状病毒(2019-nCoV)的实时逆转录酶聚合酶链反应检测结果。** 循环阈值(Ct)较低表示病毒载量较高。NT 表示未检测。
结果
2019-nCoV 的样本检测
于该患者发病第 4 日采集的初始呼吸道样本(鼻咽拭子和口咽拭子)呈 2019-nCoV 阳性(表 2)。疾病第 4 日的循环阈值(Ct)低(鼻咽样本为 18~20,口咽样本为 21~22),因此提示尽管患者的初始症状轻,但这些样本中的病毒载量高。
发病第 7 日采集的两份上呼吸道样本仍呈 2019-NcV 阳性,并且鼻咽拭子样本的病毒载量仍然高(Ct 值,23~24)。发病第 7 日采集的粪便样本也呈 2019-NcV 阳性(Ct 值,36~38)。
两个采样日期采集的血清样本均呈 2019-nCoV 阴性。
发病第 11 日和第 12 日采集的鼻咽和口咽样本显示出病毒载量下降趋势。发病第 12 日采集的口咽样本呈 2019-nCoV 阴性。我们仍在等待上述日期采集的血清样本 rRT-PCR 结果。
基因测序
口咽和鼻咽样本全基因组序列完全相同,并且与已发布的其他 2019-nCoV 序列几乎相同。在该患者的病毒和 2019-nCoV 参考序列(NC_045512.2)之间,只有位于开放阅读框 8 的 3 个核苷酸和 1 个氨基酸存在差异。该序列参见 GenBank(登录号 MN985325)[16]。
讨论
我们报告的美国首例 2019-nCoV 确诊病例说明这一新暴发的疫情有几个方面尚未完全明了,包括传播动力学和临床疾病的全疾病谱。
该患者曾前往中国武汉,但自诉在武汉期间未去过海鲜批发市场,未去过医疗机构,也未接触过任何患者。尽管其 2019-nCoV 感染的来源不明,但有关人际传播的证据已经发布。截至 2020 年 1 月 30 日,尚未发现与该病例相关的 2019-nCoV 继发病例,但对其密切接触者的监测仍在继续 [19]。
我们在患者发病第 4 日和第 7 日的上呼吸道样本中检出 2019-nCoV RNA,且 Ct 值低,因此提示病毒载量高,有传播潜力。值得注意的是,我们还在患者发病第 7 日采集的粪便样本中检出了 2019-nCoV RNA。虽然该患者血清样本的 2019-nCoV 检测结果反复呈阴性,但中国重病患者血液内已检出病毒 RNA [4]。
然而,肺外检出病毒 RNA 不一定意味着存在传染性病毒,目前尚不明确呼吸道外检出病毒 RNA 的临床意义。
目前,我们对 2019-nCoV 感染的临床谱了解非常有限。中国已报告了重度肺炎、呼吸衰竭、急性呼吸窘迫综合征(ARDS)和心脏损伤等并发症,包括致死病例 [4,18,20]。
然而,需要注意的是,这些病例是在其肺炎诊断的基础上确定的,因此报告可能偏向更严重的结局,存在偏倚。
我们的患者最初表现为轻度咳嗽和轻度间歇性发热,发病第 4 日胸片并无肺炎迹象,之后在发病第 9 日时进展为肺炎。在 2019-nCoV 感染的临床病程早期,轻度疾病的这些非特异性症状和体征在临床上与许多其他常见传染病可能无法区分,尤其是在冬季呼吸道病毒感染季。此外,该患者在发病第 9 日进展为肺炎,这一时间与最近一篇论文中报道的呼吸困难迟发相符(中位时间为发病第 8 日)[4]。
尽管我们因患者临床状况恶化而决定特许使用 remdesivir,但我们需要通过随机对照试验来确定 remdesvir 及用于治疗 2019-nCoV 感染患者的其他试验性药物的安全性和疗效。
我们在本文中报告了美国报告的首例 2019-nCoV 感染患者临床特征。该病例要点包括患者看到关于疫情的公共卫生警告后决定就医;当地医务人员了解到患者近期曾前往武汉,之后当地、州和国家公共卫生工作人员彼此协调;识别出可能有 2019-nCoV 感染,因而可以迅速隔离患者,由实验室确认 2019-nCoV 感染,并将患者收入院,进行进一步检查和治疗。
此份病例报告突显出临床医师面对因急性病症状而就诊的患者时,询问清楚近期旅行史或与其他患者接触史的重要意义,这样才能确保正确识别和迅速隔离可能有 2019-nCoV 感染风险的患者,从而减少疾病进一步传播。
最后,此份报告还突显出我们需要确定与 2019-nCoV 感染相关临床疾病的全疾病谱和自然史、发病机制以及向体外排出病毒的持续时间,从而指导临床治疗和公共卫生决策。
本文作者:Michelle L. Holshue, M.P.H., Chas DeBolt, M.P.H., Scott Lindquist, M.D., Kathy H. Lofy, M.D., John Wiesman, Dr.P.H., Hollianne Bruce, M.P.H., Christopher Spitters, M.D., Keith Ericson, P.A.-C., Sara Wilkerson, M.N., Ahmet Tural, M.D., George Diaz, M.D., Amanda Cohn, M.D., LeAnne Fox, M.D., Anita Patel, Pharm.D., Susan I. Gerber, M.D., Lindsay Kim, M.D., Suxiang Tong, Ph.D., Xiaoyan Lu, M.S., Steve Lindstrom, Ph.D., Mark A. Pallansch, Ph.D., William C. Weldon, Ph.D., Holly M. Biggs, M.D., Timothy M. Uyeki, M.D., and Satish K. Pillai, M.D. for the Washington State 2019-nCoV Case Investigation Team*
参考文献:
1. World Health Organization. Pneumonia of unknown cause — China. 2020 (https://www.who.int/csr/don/05-january-2020-pneumonia-of-unkown-cause-china/en/. opens in new tab).2. World Health Organization. Novel coronavirus — China. 2020 (https://www.who.int/csr/don/12-january-2020-novel-coronavirus-china/en/.).3. Chan JF-W, Yuan S, Kok K-H, et al. A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. Lancet 2020 January 24 (Epub ahead of print).4. Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 2020 January 24 (Epub ahead of print).5. Centers for Disease Control and Prevention. 2019 Novel coronavirus, Wuhan, China: 2019-nCoV situation summary. January 28, 2020 (https://www.cdc.gov/coronavirus/2019-nCoV/summary.html.).6. Phan LT, Nguyen TV, Luong QC, et al. Importation and human-to-human transmission of a novel coronavirus in Vietnam. N Engl J Med. DOI: 10.1056/NEJMc2001272.7. Johns Hopkins University CSSE. Wuhan coronavirus (2019-nCoV) global cases (https://gisanddata.maps.arcgis.com/apps/opsdashboard/index.html#/bda7594740fd40299423467b48e9ecf6.).8. Centers for Disease Control and Prevention. Interim guidance for healthcare professionals: criteria to guide evaluation of patients under investigation (PUI) for 2019-nCoV. 2020 (https://www.cdc.gov/coronavirus/2019-nCoV/clinical-criteria.html.).9. Centers for Disease Control and Prevention. Infection control. 2019 Novel coronavirus, Wuhan, China. 2020 (https://www.cdc.gov/coronavirus/2019-nCoV/infection-control.html.).10. Mulangu S, Dodd LE, Davey RT Jr, et al. A randomized, controlled trial of ebola virus disease therapeutics. N Engl J Med 2019;381:2293-2303.11. Sheahan TP, Sims AC, Leist SR, et al. Comparative therapeutic efficacy of remdesivir and combination lopinavir, ritonavir, and interferon beta against MERS-CoV. Nat Commun 2020;11:222-222.12. Centers for Disease Control and Prevention. Interim guidelines for collecting, handling, and testing clinical specimens from patients under investigation (PUIs) for 2019 novel coronavirus (2019-nCoV). 2020 (https://www.cdc.gov/coronavirus/2019-nCoV/guidelines-clinical-specimens.html.).13. Centers for Disease Control and Prevention, Respiratory Viruses Branch, Division of Viral Diseases. Real-time RT-PCR panel for detection 2019-novel coronavirus. 2020 (https://www.cdc.gov/coronavirus/2019-ncov/downloads/rt-pcr-panel-for-detection-instructions.pdf.).14. Centers for Disease Control and Prevention, Respiratory Viruses Branch, Division of Viral Diseases. 2019-novel coronavirus (2019-nCoV) real-time rRT-PCR panel primers and probes. 2020 (https://www.cdc.gov/coronavirus/2019-ncov/downloads/rt-pcr-panel-primer-probes.pdf.).15. Centers for Disease Control and Prevention. Information for laboratories. 2019 novel coronavirus, Wuhan, China. 2020 (https://www.cdc.gov/coronavirus/2019-nCoV/guidance-laboratories.html.).16. National Institutes of Health. GenBank overview (https://www.ncbi.nlm.nih.gov/genbank/.).17. GISAID (Global Initiative on Sharing All Influenza Data) home page (https://www.gisaid.org/.).18. Zhu N, Zhang D, Wang W, et al. A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med. DOI: 10.1056/NEJMoa2001017.19. Washington State Department of Health. Novel coronavirus outbreak 2020 (https://www.doh.wa.gov/Emergencies/Coronavirus.).20. Chen N, Zhou M, Dong X Jr, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet 2020 January 30 (Epub ahead of print).
联系我们
为更好地保障疫情防治需要,丁香通诚邀您提供相关信息,不限于:可供应产品信息、捐赠意向、技术资料等内容,请通过邮件 biomart@dxy.cn 联系我们!
直击抗疫科研前线,丁香通与你同在!
